敗血性關節炎
| 敗血性關節炎 Septic arthritis | |
|---|---|
| 又称 | 化膿性關節炎(pyogenic arthritis)、感染性關節炎(infectious arthritis)、關節感染(joint infection) |
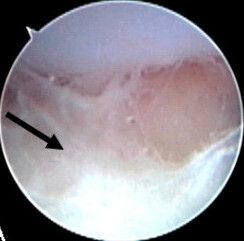 | |
| 關節鏡檢查發現敗血性關節炎[1] | |
| 症状 | 單一關節出現發紅、發熱和疼痛[2] |
| 起病年龄 | 急性發作[2] |
| 病因 | 細菌、病毒、真菌、寄生蟲[3] |
| 风险因素 | 人工關節置換術、關節炎病史、糖尿病、免疫功能低下[2] |
| 診斷方法 | 關節穿刺術與微生物培養[2] |
| 鑑別診斷 | 類風濕性關節炎、反應性關節炎、骨關節炎、痛風[2][3] |
| 治療 | 抗生素、外科手術[2] |
| 藥物 | 萬古黴素、頭孢曲松、頭孢他啶[2] |
| 预后 | 死亡風險:接受治療 15%;未治療 66%[2] |
| 患病率 | 5人/每年每十萬人[3] |
| 分类和外部资源 | |
| 醫學專科 | 風濕病學、骨外科 |
| ICD-11 | FA10 |
| ICD-9-CM | 711.95、711.93、711.90、711.9、711.94、711.91、711.0、711.92、711.97、711.96、711.40 |
| DiseasesDB | 29523 |
| MedlinePlus | 000430 |
| eMedicine | 236299 |
敗血性關節炎(英語:Septic arthritis),又作化膿性關節炎(英語:Pyogenic arthritis)或感染性關節炎(英語:Infectious arthritis),是病原體侵入關節導致的關節炎[3]。症狀通常包括單一關節發紅、發熱、疼痛、伴有關節活動能力下降[2]。發病通常很快[2]。其他症狀可能包括發燒、虛弱、頭痛[2][3]。偶爾會影響多個關節[3]。
原因包括細菌、病毒、真菌、寄生蟲[3]。危險因子包括人工關節、關節炎病史、糖尿病、免疫功能低下[2]。病原體通常由血液循環傳播到關節,但也可因外傷或關節周圍感染直接傳播到關節[2]。診斷通常需進行關節穿刺術,並將抽取的關節液進行細菌培養[2]。關節液中的白血球數量大於50,000個/mm3或乳酸濃度大於10mmol/L也可作為診斷的參考[2][4]。
初始治療通常包括萬古黴素、頭孢曲松、頭孢他啶等抗生素[2]。也可手術清理關節[2]。如果沒有及早治療,可能產生長期的關節問題[2]。每年每10萬人中約有5人得到敗血性關節炎[3]。它在老年人中更常見[3]。經治療約有15%患者會死亡,未經治療的死亡率高達66%[2]。
症狀和體徵
[编辑]敗血性關節炎常見症狀是關節處的疼痛、腫脹和發熱[2][5]。因此病患常會排斥使用四肢,使讓關節保持不動。患者也可能發燒,但是老年人發燒的比例較低[6]。
身體檢查時,應鑑別病因是源自關節內或是關節周圍(如:滑液囊和皮膚)。源自關節內的關節炎,通常會使關節活動範圍嚴重受限,關節只好維持伸展的姿勢,此姿勢的關節內空間最大。源自關節周圍感染的關節炎,只有關節活動時才會痛,且病灶通常局限於關節周圍的某一特定區域[2]。
最常發病的關節是膝[6]。髖、肩、腕、肘等關節較少患病[7]。此外,脊柱、胸鎖關節、薦髂關節也可能感染,但以上關節炎常出現在靜脈毒品注射注射者[5]。通常只有單一關節被感染。如果細菌通過血液循環傳播,則可能影響多個關節[5]。
人工關節
[编辑]接受人工關節置換的患者,膝關節感染的機率是 0.86-1.1%,髖關節感染的機率是 0.3-1.7%。人工關節感染分為三個階段:早期、遲發和晚期[2]。
- 早期 – 術後三個月內發生。常見症狀包括:發燒、關節痛和關節手術處發紅與發熱。一般是關節置換手術中發生的感染。常見的細菌是金黃色葡萄球菌和革蘭氏陰性桿菌.[2]
- 遲發 – 術後三個月至24個月間發生。由於人工關節鬆動,會出現持續的關節疼痛。一般是關節置換手術中發生的感染。常見的細菌是凝固酶陰性葡萄球菌和痤瘡丙酸桿菌(Cutibacterium acnes)[2]。
- 晚期 – 術後24個月後發生。通常會突然發生關節痛和發燒。一般是透過血液循環感染。與正常關節的敗血性關節炎菌種相同[2]。
病因
[编辑]敗血性關節炎的最常見病因是細菌感染[8]。細菌可以透過以下方式進入關節:
血液中的微生物可能來自身體其他部位的感染,例如傷口感染、泌尿道感染、腦膜炎、心內膜炎[7]。有時感染來自未知部位。由血液循環傳播的病原,特別容易感染患有關節炎(如.. 類風濕性關節炎)的關節,造成敗血性關節炎[7]。此外,有些類風濕性關節炎的治療會造成免疫功能低下,並增加感染風險[2]。靜脈用藥會造成心內膜炎,使細菌在隨血液循環四處擴散,繼而引起敗血性關節炎[2]。細菌可以透過先前的手術、關節注射、創傷、人工關節置換等方式直接進入關節[5][9][10]。
風險因素
[编辑]敗血性關節炎的發生率每10萬人年 4-29 例不等,依患者共病和關節狀況而定。敗血性關節炎患者中,85% 患者同時患有其它疾病,而其中 59% 有關節疾病史[2]。具有一個以上的危險因素會大幅增加敗血性關節炎的風險[7]。
- 年齡超過 80 歲[2][7]
- 糖尿病[2][7]
- 骨關節炎[2]
- 類風濕性關節炎[7]。使用抗腫瘤壞死因子-α藥物會增加敗血性關節炎的風險[2]。
- 免疫抑制劑[2]
- 靜脈藥物濫用[2]
- 最近進行關節手術[7]
- 髖或膝人工關節置換術和皮膚感染[2][7]
- 人類免疫缺陷病毒感染[2][7]
- 其他原因造成的敗血症[2]
病原體
[编辑]多數患者只有一種病原體感染。然而,若有大型開放性傷口,關節可能被多種病原體感染[10]。敗血性關節炎通常由細菌引起,但也可能是病毒、分枝桿菌、真菌等病原體引起。大致可以分為三類:非淋病球菌性關節炎、淋病球菌性關節炎、其他[2]。
- 非淋病球菌性關節炎 – 這些細菌佔敗血性關節炎患者 80% 以上,常見葡萄球菌或鏈球菌[2]。此類感染最常來自吸毒、蜂窩組織炎、膿瘍、心內膜炎和慢性骨髓炎[2]。感染耐甲氧西林金黃色葡萄球菌(Methicillin-resistant Staphylococcus aureus,MRSA)的可能占 5-25% 患者,而革蘭氏陰性桿菌占 14-19%。革蘭氏陰性菌感染通常源自尿路感染、藥物濫用和皮膚感染。免疫力低下的老年人也容易感染革蘭氏陰性菌。常見的革蘭氏陰性菌有:綠膿桿菌和大腸桿菌[2]。革蘭氏陽性菌和陰性菌感染通常都是由感染源通過血液傳播;但也可以直接感染關節或由關節的周圍組織傳播至關節內[5]。它常影響老年人,且多為突然發生,只感染一個關節。關節抽吸液的培養陽性率約 90%,而血液培養長任何病原菌的陽性率只有 50%[2]。
- 淋病球菌性關節炎 – 40歲以下的性活躍者中造成敗血性關節炎的常見病原是淋球菌(Neisseria gonorrhoeae)[2][5]。細菌透過性傳播後,經血液再感染關節。散佈性淋病雙球菌感染症的其它症狀包括遊走性關節痛、腱鞘炎和皮膚炎[2][10]。滑液培養的陽性率在 25-70%,但血液培養很少陽性[2]。除了血液和關節培養,應取得尿道、直腸、咽部和子宮頸的拭子培養。若診斷困難且臨床表現類似反應性關節炎,另一個有用的方法是利用聚合酶鏈式反應(Polymerase chain reaction,PCR)鑑定淋球菌感染[2]。
- 其它 – 真菌和分枝桿菌感染是敗血性關節炎的罕見病原,且通常關節症狀發作緩慢。分枝桿菌關節感染最常影響髖和膝關節,通常是過去感染的分枝桿菌的活化造成,可合併或不合併肺結核的症狀和體徵。患者中 80% 滑液培養陽性。然而,抗酸染色陽性無益於診斷。組織學變化和其他肉芽腫疾病相近,結果並無特異度[2]。引起萊姆病的伯氏疏螺旋體(Borrelia burgdorferi)能影響膝關節等多個大關節。萊姆病可以酶聯免疫吸附試驗 (Enzyme-Linked ImmunoSorbent Assay,ELISA) 篩檢,之後再以西方墨點法確認診斷。它不能在滑液中培養。然而,滑液的 PCR 檢驗 85% 陽性[2]。病毒,如:風疹、細小病毒 B19、基孔肯雅熱和人類免疫缺陷病毒,感染也能引起敗血性關節炎[5]。
- 人工關節感染 – 人工關節常由凝固酶陰性葡萄球菌、金黃色葡萄球菌和革蘭氏陰性桿菌感染。其中 20% 同時感染多種病原體。人工關節感染的危險因子包括:曾有骨折病史、血清陽性的類風濕性關節炎、肥胖、人工膝關節再置換手術和手術部位感染[2]。
病原體列表
[编辑]- 葡萄球菌屬:占 40% 患者[2]。
- 鏈球菌屬:第二常見的病原體[2][10],佔 28% 患者[2]。
- 流感嗜血桿菌[11][12]
- 淋球菌:年輕人和性活躍成年人感染敗血性關節炎的最常見原因[13]。軀幹上出現多個斑疹或水泡是淋病的特殊病徵[14]。
- 腦膜炎雙球菌[7][10]
- 大腸桿菌:常見於老人、靜脈用藥者、重病患者[7]。
- 綠膿桿菌:靜脈用藥者、穿透鞋子的穿刺外傷者[5][10]。
- 結核分枝桿菌、沙門氏桿菌和布魯氏菌:敗血性脊柱關節炎[15]。
- 囓蝕艾肯氏菌(Eikenella corrodens):人類咬傷[5]
- 多殺性巴斯德氏菌(Pasteurella multocida)、漢氏巴爾通體:動物咬傷或抓傷[5]。
- 真菌:免疫功能低下者[7]。
- 伯氏疏螺旋體:以蜱為媒介,傳染人後造成萊姆病[7]。
診斷
[编辑]| 類別 | 白血球數量/mm3 | 嗜中性白血球 % | 黏度 | 外觀 |
|---|---|---|---|---|
| 正常 | <200 | 0 | 高 | 透明 |
| 骨關節炎 | <5000 | <25 | 高 | 黃色澄清 |
| 外傷 | <10,000 | <50 | 不一定 | 血色 |
| 發炎性 | 2,000-50,000 | 50-80 | 低 | 黃色混濁 |
| 敗血性關節炎 | >50,000 | >75 | 低 | 黃色混濁 |
| 淋病性關節炎 | ~10,000 | 60 | 低 | 黃色混濁 |
| 結核性關節炎 | ~20,000 | 70 | 低 | 黃色混濁 |
| 發炎性 = 痛風、類風濕性關節炎、風溼熱 | ||||
患者出現急性單一關節腫痛,不論是否發燒,都必須優先考慮敗血性關節炎。此病症可能同時影響一個或多個關節[2][5][6]。
診斷敗血性關節炎需基於身體檢查和關節穿刺術以及時取得發炎關節的滑液。在使用抗生素前需先取得關節液,並進行革蘭氏染色、細菌培養、白血球數量及分類和結晶分析[5][7]。在性活躍者,若懷疑病原是淋球菌(N. gonorrhoeae),需包括核酸增幅試驗(NAAT)[10]。
其他應包括的檢查有:血液培養、白血球數量和類別、紅血球沉降率(ESR)和C反應蛋白(CRP)。但是,白血球數量、ESR 和 CRP 並無特異性且可能因體內其他部位感染而上升。如果懷疑萊姆病,應進行血清學檢查[5][10]。敗血性關節炎患者中,血液培養 25-50% 陽性,因為病原體是透過血液循環散播[2]。
關節抽吸檢查
[编辑]
關節液檢查,敗血性關節炎的白血球數量一般會超過 50,000-100,000/mm3[19];當超過 90% 的白血球是嗜中性顆粒球時也偏向診斷為敗血性關節炎[2]。在裝有人工關節的部位,當白血球數量超過 1,100/mm3 且嗜中性顆粒球比率超過 64% 傾向診斷為敗血性關節炎[2]。但在疾病早期,關節液(滑液)中的白血球數量可能只有數千。因此,單獨根據白血球計數是無法完全鑑別敗血性關節炎和其它問題[7][19]。滑液 PCR 分析可用於尋找較少見的生物,如:疏螺旋體(Borrelia)。此外,測量關節液中的蛋白質和葡萄糖濃度無益於診斷[2]。
革蘭氏染色陽性可以輔助診斷敗血性關節炎,但結果陰性無法完全排除診斷的可能性[7]。
在非淋病性關節炎,關節液的微生物培養陽性率起過 90%;然而,若患者在關節液培養前就開始抗生素治療,培養結果可能會是陰性[5][7]。在淋病性關節炎或病原屬於苛求性菌,則培養結果通常是陰性[5][7]。
如果培養陰性或懷疑淋球性關節炎,則關節液應進行核酸增幅試驗[5]。
結晶檢查發現結晶並無法排除敗血性關節炎。像痛風這樣的結晶性關節炎,急性發作時也可能同時併發敗血性關節炎[2]。
滑液中的乳酸濃度超過 10 mmol/L 時,診斷的可能性較高[4]。
血液檢驗
[编辑]實驗室檢查包括白血球計數、紅血球沉降率(ESR)和C反應蛋白(CRP)。敗血性關節炎患者的檢驗結果數值通常都會升高;然而,這些檢驗並無特異度,在其他感染或發炎性疾病也會升高[2][5]。前降鈣素可能比 CRP 更有參考價值[20]。
影像學
[编辑]影像(X射線、電腦斷層掃瞄、核磁共振成像和超聲波)檢查的結果並無特異度。它們有助於確定發炎的區域,但無法確認敗血性關節炎的診斷[9]。
當懷疑敗血性關節炎時,通常X射線影像檢查是必要的[7],它可以評估周圍結構中的任何問題[7],如:骨折、軟骨鈣質沈積病和發炎性關節炎等易發生敗血性關節炎的危險因子[2]。儘管 X 射線無法在早期診斷/治療中發揮作用,但可能顯示關節間隙輕微增加和周圍組織輕微腫脹[5]。晚期的變化包括因關節破壞而使關節間隙變窄[9]。
診斷並不需要電腦斷層掃瞄和核磁共振成像,但當診斷尚不明確或是關節部位難以檢查(如:薦腸關節或髖關節);他們有助於評估關節內或周圍的發炎/感染(如:骨髓炎)[7][9] ,骨侵蝕和骨髓水腫[2]。關節穿刺術也可透過 CT 和 MRI 掃瞄引導進行[2]。
鑑別診斷
[编辑]治療
[编辑]通常採用靜脈注射抗生素、鎮痛藥、清創術、關節穿刺術[5][7]。關節排出膿液很重要,可用針抽吸(穿刺術)或以手術引流(關節切開術)[2]。
疑似細菌感染即可開始經驗性抗生素治療。治療應基於滑液的革蘭氏染色和其它臨床發現[2][5]。一般準則如下:
- 革蘭氏染色陽性球菌 – 萬古黴素[2][7]
- 革蘭氏染色陰性球菌 – 頭孢曲松[2]
- 革蘭氏染色陰性桿菌 – 頭孢曲松、頭孢噻肟或頭孢他啶[7]
- 革蘭氏染色陰性且免疫能力正常 – 萬古黴素[7]
- 革蘭氏染色陰性且免疫功能低下 – 萬古黴素 + 第三代頭孢菌素[7]
- 毒品靜脈注射者(可能是綠膿桿菌)– 頭孢他啶 +/- 氨基糖苷類抗生素[5][7]
一旦細菌培養有結果,即可針於個別病原體變更抗生素[5][7]。靜脈抗生素治療反應良好後,可以改用口服抗生素。口服抗生素的療程時間長短不一,依病原體不同,一般需持續 1-4 週[2][5][7]。每日反覆進行關節穿刺能有效治療敗血性關節炎。每次抽出的液體應送檢:細菌培養、革蘭氏染色、白血球數量,以追蹤疾病的進展。傳統開放手術和關節鏡手術有助於感染關節的引流。手術中,同時可完成清除沾黏、膿液引流和壞死組織清創[2]。經常緊密追蹤,包括身體檢查和實驗室檢驗,以確定患者不再發燒、疼痛緩解、關節活動範圍改善和檢驗結果恢復正常[2][7]。
人工關節感染後,通常會在植入的人工關節表面形成一個生物薄膜,造成抗生素的抗藥性[21]。這些患者也常需進行手術清創[2][22]。在人工關節移除時,通常不會馬上換上植入新的人工關節,使抗生素充分作用,完全清除這區域的感染[9][22]。無法進行手術的患者,可能需要長期抗生素治療抑制感染[9]。在牙科、泌尿生殖道和胃腸道處置前,使用預防性抗生素是否能預防人工關節感染仍有爭議[2]。
低品質證據顯示,兒童使用皮質類固醇可能可以可以減輕疼痛和抗生素治療的天數[23]。
流行病學
[编辑]每年每10萬人中約有5人得到敗血性關節炎[3]。較常出現在老年人[3]。它在老年人中更常見。經治療約有 15% 患者會死亡,未經治療的死亡率高達 66%[2]。
結果
[编辑]關節變成永久性殘疾的風險差異很大[7]。這通常取決於出現症狀後到治療開始的期間,因為愈晚治療,感染會告成關節破壞更嚴重。感染的病原體、患者的年齡、過去的關節炎病史和其他合併症也會增加破壞的風險[9]。淋病球菌性關節炎一般不會造成長期破壞[5][7][9]。金黃色葡萄球菌的敗血性關節炎患者完成抗生素治療後,46-50% 的關節功能會恢復。在存活的肺炎球菌敗血性關節炎患者,95% 的關節功能會恢復。在有關節疾病史或人工關節植入的患者,三分之一有功能受損(包括:截肢、關節固定術、關節置換術和關節功能惡化)的風險[2]。死亡率通常在 10-20% 間[9]。死亡率會因病原體的侵襲性、患者年齡增加和類風濕關節炎等合併症而增加[7][9][10]。
參考文獻
[编辑]- ^ Hagino, Tetsuo; Wako, Masanori; Ochiai, Satoshi. Arthroscopic washout of the ankle for septic arthritis in a three-month-old boy. Sports Medicine, Arthroscopy, Rehabilitation, Therapy & Technology. 1 October 2011, 3 (1): 21. PMC 3192658
 . PMID 21961455. doi:10.1186/1758-2555-3-21.
. PMID 21961455. doi:10.1186/1758-2555-3-21.
- ^ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 2.14 2.15 2.16 2.17 2.18 2.19 2.20 2.21 2.22 2.23 2.24 2.25 2.26 2.27 2.28 2.29 2.30 2.31 2.32 2.33 2.34 2.35 2.36 2.37 2.38 2.39 2.40 2.41 2.42 2.43 2.44 2.45 2.46 2.47 2.48 2.49 2.50 2.51 2.52 2.53 2.54 2.55 2.56 2.57 2.58 2.59 2.60 2.61 2.62 2.63 2.64 2.65 2.66 2.67 2.68 2.69 2.70 2.71 2.72 2.73 2.74 2.75 Horowitz, DL; Katzap, E; Horowitz, S; Barilla-LaBarca, ML. Approach to septic arthritis.. American Family Physician. 15 September 2011, 84 (6): 653–60. PMID 21916390.
- ^ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 Arthritis, Infectious. NORD (National Organization for Rare Disorders). 2009 [19 July 2017]. (原始内容存档于21 February 2017).
- ^ 4.0 4.1 Carpenter, CR; Schuur, JD; Everett, WW; Pines, JM. Evidence-based diagnostics: adult septic arthritis.. Academic Emergency Medicine. August 2011, 18 (8): 781–96. PMC 3229263
 . PMID 21843213. doi:10.1111/j.1553-2712.2011.01121.x.
. PMID 21843213. doi:10.1111/j.1553-2712.2011.01121.x.
- ^ 5.00 5.01 5.02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 5.15 5.16 5.17 5.18 5.19 5.20 5.21 5.22 5.23 5.24 5.25 Kasper, Dennis L.; Fauci, Anthony S.; Hauser, Stephen L.; Longo, Dan L.; Larry Jameson, J.; Loscalzo, Joseph. Infectious Arthritis. Harrison's principles of internal medicine.. Kasper, Dennis L.,, Fauci, Anthony S., 1940-, Hauser, Stephen L.,, Longo, Dan L. (Dan Louis), 1949-, Jameson, J. Larry,, Loscalzo, Joseph 19th. New York. 2015. ISBN 9780071802161. OCLC 893557976.
- ^ 6.0 6.1 6.2 Margaretten, Mary E.; Kohlwes, Jeffrey; Moore, Dan; Bent, Stephen. Does this adult patient have septic arthritis?. JAMA. 2007-04-04, 297 (13): 1478–1488. ISSN 1538-3598. PMID 17405973. doi:10.1001/jama.297.13.1478.
- ^ 7.00 7.01 7.02 7.03 7.04 7.05 7.06 7.07 7.08 7.09 7.10 7.11 7.12 7.13 7.14 7.15 7.16 7.17 7.18 7.19 7.20 7.21 7.22 7.23 7.24 7.25 7.26 7.27 7.28 7.29 7.30 7.31 7.32 7.33 7.34 7.35 7.36 7.37 7.38 7.39 7.40 7.41 Goldberg, D.L.; Sexton, D.J. Septic arthritis in adults. UpToDate. Waltham, MA: UpToDate Inc. 2017. (原始内容存档于2019-11-08).
- ^ Shirtliff, Mark E.; Mader, Jon T. Acute Septic Arthritis. Clinical Microbiology Reviews. October 2002, 15 (4): 527–544. ISSN 0893-8512. PMC 126863
 . PMID 12364368. doi:10.1128/CMR.15.4.527-544.2002.
. PMID 12364368. doi:10.1128/CMR.15.4.527-544.2002.
- ^ 9.00 9.01 9.02 9.03 9.04 9.05 9.06 9.07 9.08 9.09 9.10 9.11 Shirtliff, Mark E.; Mader, Jon T. Acute Septic Arthritis. Clinical Microbiology Reviews. 2002-10-01, 15 (4): 527–544. ISSN 0893-8512. PMC 126863
 . PMID 12364368. doi:10.1128/cmr.15.4.527-544.2002.
. PMID 12364368. doi:10.1128/cmr.15.4.527-544.2002.
- ^ 10.00 10.01 10.02 10.03 10.04 10.05 10.06 10.07 10.08 10.09 10.10 10.11 10.12 Osteomyelitis and Septic Arthritis. Principles and practice of hospital medicine. McKean, Sylvia C.,, Ross, John J. (John James), 1966-, Dressler, Daniel D.,, Scheurer, Danielle Second. New York: McGraw-Hill Education. 2017. ISBN 9780071843133. OCLC 950203123.
- ^ Bowerman SG, Green NE, Mencio GA. Decline of bone and joint infections attributable to haemophilus influenzae type b. Clin. Orthop. Relat. Res. August 1997, (341): 128–33 [2019-11-08]. PMID 9269165. (原始内容存档于2012-03-11).
- ^ Peltola H, Kallio MJ, Unkila-Kallio L. Reduced incidence of septic arthritis in children by Haemophilus influenzae type-b vaccination. Implications for treatment. J. Bone Joint Surg. Br. May 1998, 80 (3): 471–3. PMID 9619939. doi:10.1302/0301-620X.80B3.8296.
- ^ Malik S, Chiampas G, Leonard H. Emergent evaluation of injuries to the shoulder, clavicle, and humerus. Emerg Med Clin North Am. November 2010, 28 (4): 739–63. PMID 20971390. doi:10.1016/j.emc.2010.06.006.
- ^ Kaandorp CJ, Dinant HJ, van de Laar MA, Moens HJ, Prins AP, Dijkmans BA. Incidence and sources of native and prosthetic joint infection: a community based prospective survey. Ann. Rheum. Dis. August 1997, 56 (8): 470–5. PMC 1752430
 . PMID 9306869. doi:10.1136/ard.56.8.470.
Weston VC, Jones AC, Bradbury N, Fawthrop F, Doherty M. Clinical features and outcome of septic arthritis in a single UK Health District 1982-1991. Ann. Rheum. Dis. April 1999, 58 (4): 214–9. PMC 1752863
. PMID 9306869. doi:10.1136/ard.56.8.470.
Weston VC, Jones AC, Bradbury N, Fawthrop F, Doherty M. Clinical features and outcome of septic arthritis in a single UK Health District 1982-1991. Ann. Rheum. Dis. April 1999, 58 (4): 214–9. PMC 1752863  . PMID 10364899. doi:10.1136/ard.58.4.214.
. PMID 10364899. doi:10.1136/ard.58.4.214.
- ^ O'Callaghan C, Axford JS. Medicine 2nd. Oxford: Blackwell Science. 2004. ISBN 978-0-632-05162-5.
- ^ Flynn, John A.; Choi, Michael J.; Wooster, L. Dwight. Oxford American Handbook of Clinical Medicine. OUP USA. 2013: 400. ISBN 978-0-19-991494-4 (英语).
- ^ Seidman, Aaron J.; Limaiem, Faten, Synovial fluid examination, StatPearls (StatPearls Publishing), 2019 [2019-12-19], PMID 30725799
- ^ Kocher, Mininder S.; Mandiga, Rahul; Murphy, Jane M.; Goldmann, Donald; Harper, Marvin; Sundel, Robert; Ecklund, Kirsten; Kasser, James R. A clinical practice guideline for treatment of septic arthritis in children: efficacy in improving process of care and effect on outcome of septic arthritis of the hip. The Journal of Bone and Joint Surgery. American Volume. June 2003, 85–A (6): 994–999. ISSN 0021-9355. PMID 12783993.
- ^ 19.0 19.1 Courtney, Philip; Doherty, Michael. Joint aspiration and injection and synovial fluid analysis. Best Practice & Research Clinical Rheumatology. 2013, 27 (2): 137–169. PMID 23731929. doi:10.1016/j.berh.2013.02.005.
- ^ Zhao, J; Zhang, S; Zhang, L; Dong, X; Li, J; Wang, Y; Yao, Y. Serum procalcitonin levels as a diagnostic marker for septic arthritis: A meta-analysis.. The American Journal of Emergency Medicine. August 2017, 35 (8): 1166–1171. PMID 28623003. doi:10.1016/j.ajem.2017.06.014.
- ^ Berbari, Elie; Baddour, L. M. Prosthetic joint infection: Epidemiology, clinical manifestations, and diagnosis. UpToDate. Waltham, MA: UpToDate Inc. 2017. (原始内容存档于2019-12-31).
- ^ 22.0 22.1 Barbari, Elie; Baddour, L. M. Prosthetic joint infection: Treatment. UpToDate. Waltham, MA: UpToDate, Inc. 2017. (原始内容存档于2019-12-31).
- ^ Delgado-Noguera, Mario F; Forero Delgadillo, Jessica M; Franco, Alexis A; Vazquez, Juan C; Calvache, Jose Andres. Corticosteroids for septic arthritis in children. Cochrane Database of Systematic Reviews. 2018-11-21, 11: CD012125. ISSN 1465-1858. PMC 6517045
 . PMID 30480764. doi:10.1002/14651858.cd012125.pub2.
. PMID 30480764. doi:10.1002/14651858.cd012125.pub2.
其他文獻
[编辑]- Resnick, Donald. Bone and joint imaging. Philadelphia: Saunders. 1989: 744–749. ISBN 0721622151.
- Bredella, Miriam A.; Stoller, David W.; Tirman, Phillip F. J. Diagnostic imaging. Salt Lake City, Utah: Amirsys. 2004: 4–99. ISBN 0-7216-2920-2.
- Edwards MS. "Osteomyelitis and Septic Arthritis"
