重鉻酸鈉
外觀
| 重鉻酸鈉 | |
|---|---|
| |

| |
| 別名 | 紅礬鈉 |
| 識別 | |
| CAS號 | 7789-12-0 10588-01-9 |
| PubChem | 25408 |
| ChemSpider | 23723 |
| SMILES |
|
| InChI |
|
| InChIKey | KIEOKOFEPABQKJ-RXLKZJBDAW |
| UN編號 | 3288 |
| EINECS | 234-190-3 |
| ChEBI | 39483 |
| RTECS | HX7750000 |
| 性質 | |
| 化學式 | Na2Cr2O7·2H2O |
| 摩爾質量 | 298.02 (二水) g·mol⁻¹ |
| 密度 | 2.52 g/cm3 |
| 熔點 | 356.7 °C 100 °C時失去結晶水 |
| 沸點 | 分解 |
| 溶解性(水) | 2380 g/L, 0 °C |
| 危險性 | |
| 警示術語 | R:R45, R46, R60, R61, R8, R21, R25, R26, R34, R42/43, R48/23, R50/53, |
| 安全術語 | S:S53, S45, S60, S61 |
| 主要危害 | 致癌 |
| NFPA 704 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
50 mg/kg |
| 相關物質 | |
| 相關化學品 | K2Cr2O7、Na2CrO4、KMnO4、CrO3 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
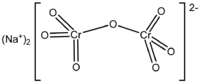
重鉻酸鈉是一種無機化合物,俗稱紅礬鈉,化學式為Na2Cr2O7,橘紅色晶體,常以二水合物的形式(Na2Cr2O7·2H2O)使用。其化學性質與重鉻酸鉀類似,在水中的溶解度約是後者的20倍(49 g/L、0 °C),相對分子質量更小,[1]然而其應用卻不及重鉻酸鉀廣泛。
有機化學應用
[編輯]重鉻酸鈉可將苄基和烯丙基化合物氧化為相應的羰基化合物,如與2,4,6-三硝基甲苯反應生成羧酸,[2]與2,3-二甲基萘反應生成2,3-萘二甲酸(熔點239–241 °C)。[3]
重鉻酸鈉亦是一種氧化劑,可以將一級醇、二級醇、醛等有機物氧化。
安全
[編輯]無水重鉻酸鈉有劇毒。[5]
參考文獻
[編輯]- ^ Freeman, F. "Sodium Dichromate" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
- ^ Clarke, H. T.; Hartman, W. W. (1941). "2,4,6-Trinitrobenzoic Acid". Org. Synth.; Coll. Vol. 1: 543.
- ^ Friedman, L. (1973). "2,3-Naphthalenedicarboxylic Acid". Org. Synth.; Coll. Vol. 5: 810.
- ^ ILO 1369 - Sodium Dichromate [1] (頁面存檔備份,存於網際網路檔案館)
- ^ 中国化工报 2008年11月12日. [2014年8月14日]. (原始內容存檔於2014年8月14日).

