氢键催化

氢键催化是一种依赖于氢键相互作用加速和控制有机反应的有机催化。生物系统中,无论是在底物分子的定向还是在降低反应壁垒方面,氢键在诸多酶促反应里都起着关键的作用。 [1]而化学方面直到最近才开始尝试利用氢键进行催化,与路易斯酸催化的研究相比,该领域尚且不发达。 [2]
催化剂量的氢键供体可以通过多种不同的机制促进反应。反应过程中,氢键可用于稳定阴离子中间体和过渡态。一些催化剂可以结合较小的阴离子,从而形成反应性的亲电阳离子。酸性更强的供体可以作为一般酸或特定酸,通过质子化激活亲电试剂。一种强有力的方法是同时激活反应中的两个部分,如亲核试剂和亲电试剂,称之为“双功能催化”。这些情况下催化剂分子与底物的紧密结合也使氢键催化成为一种强大的诱导对映选择性的方法。
氢键催化剂通常制造简单,相对稳健,并且可以以高对映体纯度合成。由氢键供体催化的新反应正越来越快被发现,包括合成常见有机反应的不对称变体,例如醛醇加成、 Diels-Alder环加成和Mannich反应等。 [3]
然而,氢键催化在合成效用方面发挥全部潜力之前,也面临几个挑战。当前已知的反应非常特定于底物的并且通常表现出低速率,因此需要高催化剂负载量。催化剂往往通过反复试验和优化,化学家对催化剂结构与反应性之间的关系了解甚少。此外,该领域中,新反应的发现已经遥遥领先于对于机理的一般理解。随着未来对结构和机理的更详细研究,氢键催化在实现新的、高效的、选择性的反应和不对称合成中的应用方面具有巨大潜力。
催化策略
[编辑]四面体中间体的稳定
[编辑]许多有机反应通过对醛、酰胺或亚胺等官能团亲核攻击而形成四面体中间体。在这些情况下适合使用氢键供体进行催化,因为阴离子四面体中间体相比原始的化合物更容易形成氢键。对于最初的催化剂-底物复合物,带有更多负电荷的过渡态更加稳定。

例如在典型的酰基取代反应中,起始的羰基化合物通过一个、两个或以上的氢键与催化剂配位。在亲核试剂攻击的过程中,负电荷集中在氧上,直至形成四面体中间体。由于负电荷增加,形式上的负氧比刚开始羰基的氧可以形成更强的氢键。在能量上,催化剂降低中间态和过渡态的能量,从而加速反应。
这种催化模式存在于丝氨酸蛋白酶等许多酶的活性位点。[4]例如在这反应中,酰胺的羰基与两个N-H供体配位。这些促进生物学中羰基反应的多重配位位点被称为“负氧离子洞”。丝氨酸亲核试剂促进形成四面体中间体,其通过增加与负氧离子洞的氢键键合而稳定下来。

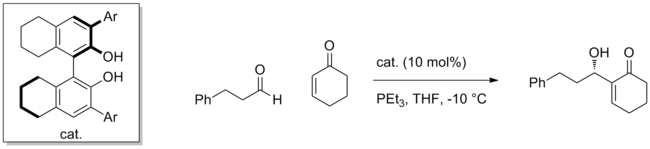
许多合成催化剂成功利用这种策略激活亲电试剂。例如使用手性的联萘酚可以高对映选择性地进行烯酮加成到醛上的贝里斯-希尔曼反应。 [5]亲核试剂由 PEt 3与烯酮共轭加成产生的烯醇化物,对映选择性地加成与催化剂配位的醛。
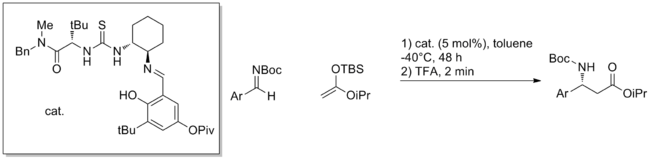
除羰基外,如亚胺的其他亲电试剂也得到应用。例如,使用简单的手性硫脲催化剂,芳族亚胺与甲硅烷基乙烯酮缩醛的不对称曼尼希反应可以以高ee近乎定量转化。 [6]该反应的机理尚未完全阐明,并且该反应具有很强的底物特异性,仅对某些芳香族亲电子试剂有效。
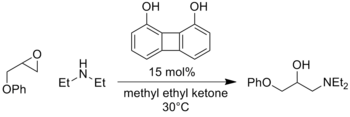
这种活化模式广泛适用,关于亲电试剂、亲核试剂和催化剂结构的不同组合的新报道纷至沓来。此外,该策略也可以成功催化氧阴离子中间体的类似反应,例如亚硝基化合物中的烯醇化物的加成[7]或环氧化物的开环[8] 。
尽管已知的不同反应众多,对催化模式的理解有限,并且几乎所有催化反应的底物特异性都极强。
阴离子的稳定
[编辑]另一种已知的策略是稳定过渡态产生的部分负电荷。反应过程中一个片段产生部分电负性,过渡态通过接受氢键而稳定。
Jacobsen组报道了酯取代烯丙基乙烯基醚的Claisen 重排催化。 [9]手性胍催化剂成功促进了接近室温的反应,具有高对映选择性。过渡态与脒鎓催化剂配位的片段由于氧的电负性和吸电子酯基团而表现出部分阴离子特性,增加了氢键的强度并降低了过渡态能量,从而加速反应。

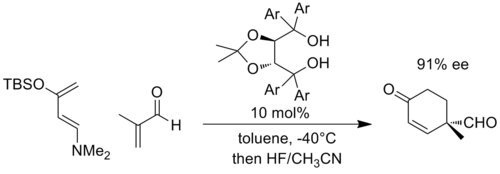
而且,诸如Diels-Alder反应的环加成反应中也可以通过负电荷的稳定达到。例如,Rawal等人开发了一种基于α,α,α,α-四芳基-1,3-二氧戊环-4,5-二甲醇 ( TADDOL ) 的手性催化剂,可以催化Diels-Alder反应。在下面的例子中,与高度富电子的双烯和贫电子的亲双烯体的反应可能在烯醇上产生显着的负电荷,并且过渡态通过增加与 TADDOL的氢键来稳定(Ar =1-萘基)。 [10]
阴离子结合
[编辑]氢键催化剂还可以通过吸附和/或配位诸如卤化物的阴离子,形成亲电物质来加速反应。尿素和硫脲催化剂是通过结合阴离子催化最常见的供体,它们结合卤化物和其他阴离子的能力已经得到充分证实。 [11]手性阴离子结合催化剂可以产生不对称的离子对,诱导反应的立体选择性。
通过阴离子结合催化的第一个反应是在硫脲催化下羟基内酰胺与TMSCl的皮克特-施彭格勒环化。[12]机理中羟基被氯化物取代后,形成了关键的离子对。手性硫脲通过亚胺与氯化物紧密结合,高立体选择性形成分子内环化。
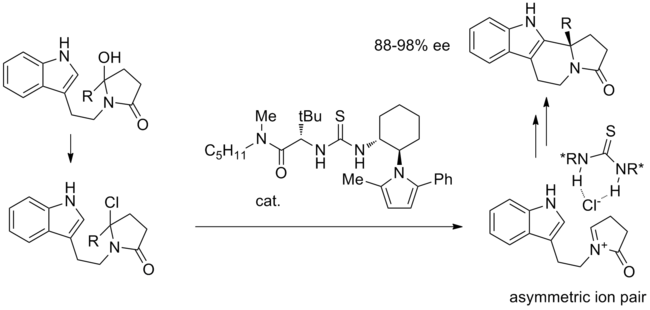
不对称离子对也可能在分子间反应中受到攻击。例如烯醇硅烷亲核试剂与氧代碳鎓离子的不对称加成可以通过阴离子结合催化形成氧代碳鎓实现。 [13]乙缩醛开始,氯醚与三氯化硼生成并与烯醇硅烷和催化剂反应。氧代碳鎓-硫脲-氯化物络合物的形成机理尚未完全解决。在该反应条件下,氯醚可以差向异构化,而硫脲可以立体选择性地结合氯化物,形成紧密缔合的离子对。该不对称离子对之后收到硅烷攻击产生烷基化产物。

阴离子结合机制的另一个例子是下图所示的由Jacobsen的酰胺基硫脲催化剂催化亚胺氢氰化反应。该反应是通过计算、光谱、标记以及动力学研究最广泛的反应之一。 [14]虽然考虑了将氰化物直接添加到催化剂结合的亚胺中,但计算出另一种机制,包括形成亚胺-氰化物离子对,其势垒可以低 20 kcal/mol。提出的最可能的机制始于催化剂与 HNC 的结合,HNC 与HCN处于平衡状态。然后该复合物使亚胺分子质子化,形成亚胺-氰化物离子对,催化剂结合并稳定氰化物阴离子。亚胺鎓也被认为与催化剂分子上的酰胺羰基相互作用(见下文双功能催化)。结合的氰化物阴离子旋转,通过碳攻击亚胺。研究人员尽管通过光谱学观察到亚胺-尿素结合并得到早期动力学实验的支持,但亚胺结合是非循环的,所有证据都指向这种涉及硫脲结合氰化物的机制。

质子化
[编辑]氢键催化和一般酸催化通常情况下很难区分。 [3]氢键供体可以具有不同的酸度,从弱到强的布仑斯惕-劳里酸,如磷酸。测定反应过程中质子转移的程度具有挑战性,并且大多数反应尚未得到彻底的研究。然而,强酸催化剂通常与氢键催化剂归为一类,因为其代表连续体的一个极端情况,并且两者的催化行为也有相似之处。这些反应的活化机制涉及亲电子物质的初始质子化,使底物更具亲电性并产生离子对,通过该离子对可以传输立体化学信息。

底物几乎完全质子化的不对称催化在芳族醛亚胺与碳亲核试剂的曼尼希反应中有效。 [15]此外,呋喃氮杂傅-克反应、重氮羰基化合物的酰胺烷基化、醛亚胺的不对称氢膦酰化以及转移氢化都有报道。 [3]手性布朗斯台德酸通常很容易从手性醇(如 BINOL)制备,并且由于它们在分子研究中已确立的实用性,文献中也有报道。 [16]
多功能策略
[编辑]氫鍵催化的主要優點之一是能夠構建參與多種非共價相互作用以促進反應的催化劑。除了在反應過程中使用氫鍵供體激活或穩定反應中心外,還可以引入其他官能團,例如路易斯碱、芳烴或加成氫鍵位點,以提供額外的穩定性或影響其他反應伴侶。
例如,天然酶双功能酶分支酸变位酶催化分支酸的克莱森重排,除了參與穩定烯醇化物樣片段的氫鍵外,還具有許多其他相互作用,這是上面討論的陰離子片段穩定策略的一個例子。 [17]一个关键的相互作用是通过过渡态的阳离子-π相互作用稳定另一个阳离子烯丙基。使許多額外的氫鍵有幾個可能目標。多個氫鍵與酶的穩定有助於克服結合的熵成本。此外,相互作用有助於將底物保持在反應性構象中,並且酶催化反應的活化熵接近於零,而溶液中典型的克萊森重排具有非常負的活化熵。

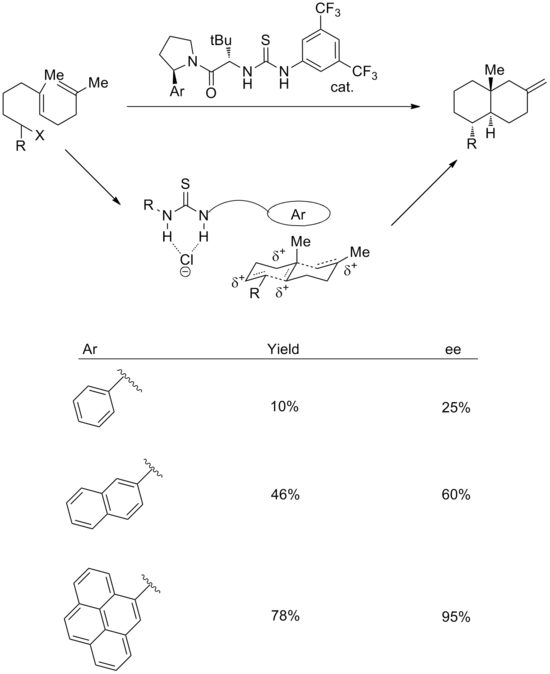
陽離子-π相互作用的使用也已成功地應用於合成催化劑的反應中。陰離子結合和陽離子π策略的組合可用於實現對映選擇性陽離子多環化。[18]在過渡態,可能機理為硫脲基團結合氯,而芳香族系統穩定相關的多烯陽離子。支持這一點的是,增加芳環的大小可提高產率和立體選擇性。對映選擇性與芳基的極化率和四極矩密切相關。
由於如此大量的催化劑和反應涉及與親電子試劑結合以穩定過渡態,因此許多雙功能催化劑還存在路易斯鹼性氫鍵受體位點。作為一個代表性的例子,Deng等人開發了一種能夠促進立體選擇性邁克爾反應的硫脲-胺催化劑。 [19]在可能的過渡態中,其中一個硫脲 N-H 供體與邁克爾受體配位,並將穩定負電荷的積累。鹼性孤對氮作為氫鍵受體配位親核試劑,但在過渡態作為一般鹼基促進親核烯醇加成。

这种让亲核和亲电伙伴参与反应并将它们稳定在过渡态,常见于硫脲有机催化文章中。
使用合成寡肽進行催化的一種相對較新的策略已經產生了許多成功的催化方法。[20]肽具有多個潛在的氫鍵位點,通常不了解這些位點如何與底物結合或如何促進反應。肽具有高度模塊化的優勢,並且通常在大型陣列中篩選這些催化劑。以這種方式已經發現了高度對映選擇性的反應,例如下面描述的羥醛反應。
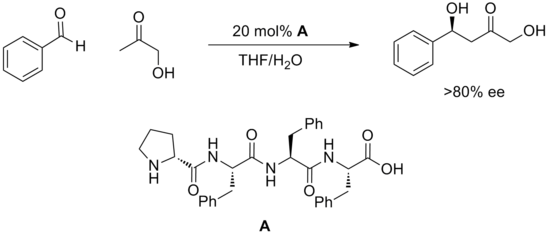
合成肽成功催化的其他轉化包括氫氰化、酰化、共軛加成、醛-亞胺偶聯、羥醛反應和溴化。雖然過渡態的性質尚不清楚,但在許多例子中,催化劑結構的微小變化對反應活性有顯著影響。據推測,肽內以及催化劑與底物之間的大量氫鍵必須合作以滿足成功催化的幾何要求。除此之外,對催化劑設計和機制的理解還沒有超出需要測試肽庫的範圍。
催化剂设计
[编辑]优选结构
[编辑]催化中使用的氫鍵供體類型因反應而異,即使在相似的催化策略中也是如此。雖然特定係統經常被廣泛研究和優化,但對反應的最佳供體或催化劑結構與反應性之間的關係的一般理解卻非常缺乏。合理設計結構以促進具有所需選擇性的所需反應尚不切實際。然而,當代氫鍵催化主要集中在少數幾種系統上,這些系統在實驗上似乎在各種情況下都有效。 [21]这些被称为“优选结构”。然而,值得注意的是,其他结构支架和图案也显示出有希望的结果,例如金属配位的氢键供体。 [22]
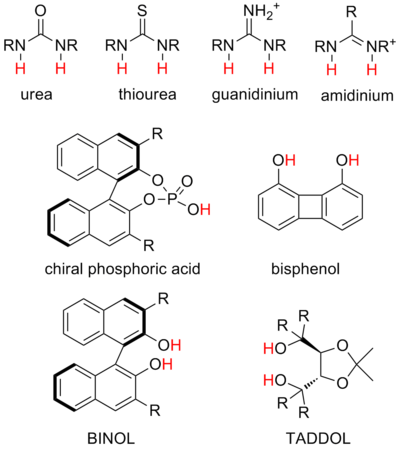
- 脲和硫脲是迄今为止最常見的結構,可以穩定多種帶負電荷的中間體,並參與陰離子結合催化。雙功能尿素和硫脲催化常见于文獻中。
- 胍和脒離子与脲和硫脲結構类似,可以催化類似的反應,但由於它們的正電荷,它們是更強的供體並且酸性更強。胍和脒催化的機制被認為通常涉及底物的部分質子化。
- 人们认为二醇催化劑通過單個氫鍵與底物結合,而另一個羥基則參與內部氫鍵。這些是最早研究的一些氫鍵催化劑。它們最常用於穩定過渡態的部分陰離子電荷,例如在異-Diels-Alder 反應中與醛親二烯體配位。
- 磷酸催化劑是最常見的強酸催化劑,通過與亞胺等鹼性底物形成手性離子對起作用。
催化剂调整
[编辑]一般来说,供体部位的酸度与供体的强度密切相关。例如,在硫脲催化剂上添加吸电子芳基取代基是一种常见的策略,这可以增加其酸性,从而增加其氢键强度。然而,目前尚不清楚供体强度与所需反应性之间的关系。重要的是,更多的酸性催化剂不一定更有效。例如,尿素的酸性比硫脲低大约 6 个 pKa 单位,但通常来说尿素的催化反应要差得多。 [23]
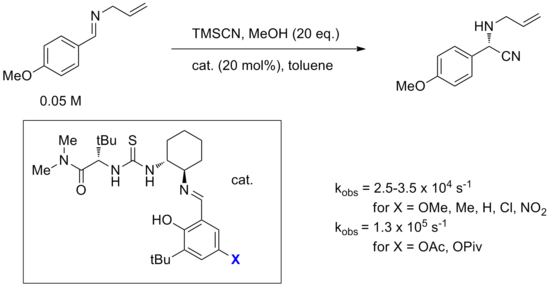
此外,人們很少了解不同取代基對催化劑的影響。小的取代基變化可以完全改變反應性或選擇性。這方面的一個例子是雙功能 Strecker 反應催化劑的優化研究,它是最早得到充分研究的硫脲催化劑之一。 [24]具體來說,改變水楊醛亞胺取代基上的 X 取代基,發現典型的吸電子或給電子取代基對速率影響很小,但酯取代基如乙酸酯或新戊酸酯似乎會引起明顯的速率加速。鑑於 X 基團在反應過程中遠離反應中心,並且電子學似乎不是原因,因此很難合理化這一觀察結果。總的來說,儘管使用有機催化劑進行電子調諧相對容易,但化學家尚未對這些修飾形成有用的理解。
合成应用
[编辑]天然产物合成
[编辑]迄今為止,儘管發現了大量反應,但在天然產物的合成中很少有氫鍵催化的例子。通常,由於需要高催化劑負載和通常極端的底物特異性,氫鍵催化尚未發展到足以提供有用的一般反應,這些反應代表了對傳統方法的顯著改進。在已發表工作中,氫鍵催化主要用於起始階段,以快速獲得對映體富集度高的早期中間體。
在 (+)-yohimbine 的 Jacobsen 合成中, [25]一種吲哚生物鹼,使用吡咯取代的硫脲催化劑的早期對映選擇性 Pictet-Spengler 反應以 94% ee 和 81% 產率產生克级產物。合成的其餘部分很短,使用還原胺化和分子內 Diels-Alder 反應。

2008 年,Takemoto 公開了 (−)-epibatidine 的簡明合成,過程依賴於由雙功能催化劑催化的邁克爾級聯。 [26]在对β-硝基苯乙烯進行初始不對稱邁克爾加成後,分子內邁克爾加成提供 75% ee 的環酮酯產物。標準官能團操作和分子內環化產生天然產物。

构建区块的可扩展合成
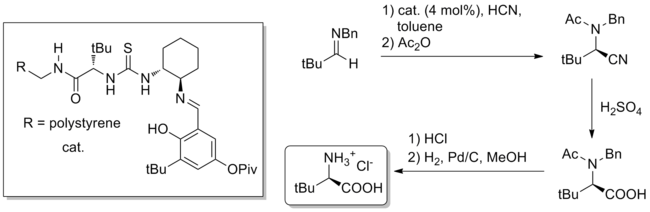
[编辑]除了全合成,氫鍵催化的一個潛在有用的應用是難以獲得的手性小分子的批量合成。一個值得注意的例子是 2009 年自然雜誌報導的使用硫脲催化的克级斯特雷克氨基酸合成反应非天然氨基酸。 [27]催化剂,无论是聚合物结合的还是均相的,都来源于天然的叔亮氨酸,可催化(4 mol% 催化劑負載)由二苯甲基胺和 HCN 水溶液形成 Strecker 產物。腈水解和脫保護以 84% 的總產率和 99% ee 產生純非天然叔亮氨酸。
挑战和展望
[编辑]儘管人們對有機催化有著廣泛的興趣,並且不斷發現大量新的催化體系,但在氫鍵催化領域對機理和催化劑設計的理解進展極為有限。与钯催化偶联反应等更发达的領域相比,氫鍵催化提出了許多尚未成功解決的挑戰。
- 剂量:虽然钯催化反应通常在催化剂负载量小于 0.1 mol %可有效,氢键催化剂的加入量往往大于10 mol %。速率加速不良是一个普遍趋势,必须克服这一趋势才能使氢键催化成为一种实用的合成策略。
- 机制:未來,需要進一步研究氫鍵催化機制中涉及的精確步驟,這將使化學家能夠合理地設計催化策略以實現更複雜或更有用的轉化。相比之下,鈀催化交叉偶聯的基本步驟在過去幾十年中得到了系統和深入的研究,並在催化範圍、控制和反應設計原則方面取得了巨大進步。例如,对氧化加成的深入了解使芳基氯成為實用的偶聯劑,而對還原消除的深入了解則促進了涉及 sp3中心的新反應的發展。了解這些基本的催化步驟,合理規劃新反應和級聯的能力在全合成領域非常有用。相比之下,我們缺乏對氫鍵催化步驟以及如何影響它們的一般、系統的機制理解。到目前為止,詳細的機理研究僅限於單個系統,他們的發現還沒有可證明的預測用途。
- 催化:一個相關的挑戰是研究如何使用催化劑、結構、構象和電子的變化來合理地影響反應。目標是充分了解如何使用多種合作相互作用來最好地加速反應並賦予選擇性。理想情況下,合理的催化劑設計最終將取代對催化劑家族的篩選,並且結構單元的選擇將變得更加系統化。
- 普适性:虽然新反應不斷被發現,但大多數反應的底物範圍都非常狹窄,而且範圍如此狹窄的原因往往不為人所知。在鈀催化領域,在建立了機理理解的基礎後,反應範圍迅速擴大。了解影響每個催化步驟的因素使化學家能夠設想和追求具有高合成效用的新反應,例如 CH 鍵活化反應。在氫鍵催化領域,化學家尚未達到可以輕鬆、系統地確定新型反應性的階段。在這一點上,反應發現是有用的,但需要更詳細的機理研究才能充分發揮氫鍵催化的潛力。
相关
[编辑]参考
[编辑]- ^ Jacobsen, E. N.; Knowles, R. R. Attractive noncovalent interactions in asymmetric catalysis: Links between enzymes and small molecule catalysts (PDF). Proc. Natl. Acad. Sci. September 2010, 107 (48): 20678–20685 [2023-05-23]. Bibcode:2010PNAS..10720678K. PMC 2996434
 . PMID 20956302. doi:10.1073/pnas.1006402107. (原始内容存档 (PDF)于2023-01-06).
. PMID 20956302. doi:10.1073/pnas.1006402107. (原始内容存档 (PDF)于2023-01-06).
- ^ Jacobsen, E. N.; Taylor, M. S. Asymmetric catalysis by chiral hydrogen-bond donors. Angew. Chem. Int. Ed. February 2006, 45 (10): 1521–1539. PMID 16491487. doi:10.1002/anie.200503132.
- ^ 3.0 3.1 3.2 Doyle, Abigail G.; Jacobsen, E. N. Small-molecule H-bond donors in asymmetric catalysis. Chem. Rev. December 2007, 107 (12): 5713–5743. PMID 18072808. doi:10.1021/cr068373r.
- ^ Sinnott, M. Comprehensive Biological Catalysis, Vol. 1. London: Academic Press. 1998: 345–379.
- ^ McDougal, N. T.; Shaus, S. E. Asymmetric Morita−Baylis−Hillman reactions catalyzed by chiral Brønsted acids. J. Am. Chem. Soc. September 2003, 125 (40): 12094–12095. PMID 14518986. doi:10.1021/ja037705w.
- ^ Wenzel, A. G.; Jacobsen, E. N. Asymmetric catalytic Mannich reactions catalyzed by urea derivatives: enantioselective synthesis of β-aryl-β-amino acids. J. Am. Chem. Soc. 2002, 124 (44): 12964–12965. PMID 12405820. doi:10.1021/ja028353g.
- ^ Yamamoto, H.; Momiyama, N. Bronsted acid catalysis of achiral enamines for regio- and enantioselective nitroso aldol Synthesis. J. Am. Chem. Soc. September 2004, 127 (4): 1080–1081. PMC 1460970
 . PMID 15669829. doi:10.1021/ja0444637.
. PMID 15669829. doi:10.1021/ja0444637.
- ^ Hine, J.; Linden, S. M.; Kanagasabapathy, V. M. Double-hydrogen-bonding catalysis of the reaction of phenyl glycidyl ether with diethylamine by 1,8-biphenylenediol. J. Org. Chem. December 1985, 50 (25): 5096–5099. doi:10.1021/jo00225a021.
- ^ Uyeda, C.; Jacobsen, E. N. Enantioselective Claisen rearrangements with a hydrogen-bond donor catalyst. J. Am. Chem. Soc. July 2008, 130 (29): 9228–9229. PMC 2547484
 . PMID 18576616. doi:10.1021/ja803370x.
. PMID 18576616. doi:10.1021/ja803370x.
- ^ Rawal, Viresh H.; Thadani, A.N.; Stankovich, A.R. Enantioselective Diels-Alder reactions catalyzed by hydrogen bonding. PNAS. 2004, 101 (16): 5846–5850. Bibcode:2004PNAS..101.5846T. PMC 395998
 . PMID 15069185. doi:10.1073/pnas.0308545101.
. PMID 15069185. doi:10.1073/pnas.0308545101.
- ^ Schmidtchen, F. P.; Berger, M. Artificial organic host molecules for anions. Chem. Rev. August 1997, 97 (5): 1609–1646. PMID 11851460. doi:10.1021/cr9603845.
- ^ Raheem, I. T.; Thiara, P. S.; Peterson, E. A.; Jacobsen, E. N. Enantioselective Pictet-Spengler-type Cyclizations of Hydroxylactams: H-Bond Donor Catalysis by Anion Binding. J. Am. Chem. Soc. August 2007, 129 (44): 13404–13405. PMID 17941641. doi:10.1021/ja076179w.
- ^ Reisman, S. E.; Doyle, A. G. Enantioselective thiourea-catalyzed additions to oxocarbenium ions. J. Am. Chem. Soc. May 2008, 130 (23): 7198–7199. PMC 2574628
 . PMID 18479086. doi:10.1021/ja801514m.
. PMID 18479086. doi:10.1021/ja801514m.
- ^ Zuend, S. J.; Jacobsen, E. N. Mechanism of amido-thiourea catalyzed enantioselective imine hydrocyanation: transition state stabilization via multiple non-covalent interactions. J. Am. Chem. Soc. September 2009, 131 (42): 15358–15374. PMC 2783581
 . PMID 19778044. doi:10.1021/ja9058958.
. PMID 19778044. doi:10.1021/ja9058958.
- ^ Uraguchi, D.; Terada, M. Chiral Brønsted acid-catalyzed direct Mannich reactions via electrophilic activation. J. Am. Chem. Soc. April 2004, 126 (17): 5356–5357. PMID 15113196. doi:10.1021/ja0491533.
- ^ Jansen, A. C. A.; Brussee, J. A highly stereoselective synthesis of s(−)-[1,1'-binaphthalene]-2,2'-diol. Tetrahedron Lett. May 1983, 24 (31): 3261–3262. doi:10.1016/S0040-4039(00)88151-4.
- ^ Lee, A.; Stewart, J. D.; Clardy, J.; Ganem, B. New insight into the catalytic mechanism of chorismate mutases from structural studies. Chemistry & Biology. April 1995, 2 (4): 195–203. PMID 9383421. doi:10.1016/1074-5521(95)90269-4
 .
.
- ^ Knowles, R. R.; Lin, S.; Jacobsen, E. N. Enantioselective thiourea-catalyzed cationic polycyclizations. J. Am. Chem. Soc. April 2010, 132 (14): 5030–5032. PMC 2989498
 . PMID 20369901. doi:10.1021/ja101256v.
. PMID 20369901. doi:10.1021/ja101256v.
- ^ Wang, B.; Wu, F.; Wang, Y.; Liu, X.; Deng, L. Control of diastereoselectivity in tandem asymmetric reactions generating nonadjacent stereocenters with bifunctional catalysis by Cinchona alkaloids. J. Am. Chem. Soc. January 2007, 129 (4): 768–769. PMID 17243806. doi:10.1021/ja0670409.
- ^ Wennemers, Helma. Asymmetric catalysis with peptides. Chem. Commun. 2011, 47 (44): 12036–12041. PMID 21993353. doi:10.1039/C1CC15237H.
- ^ Dalko, P. I. Enantioselective organocatalysis. Weinheim: Wiley-VCH. 2007. ISBN 978-3-527-31522-2.
- ^ Xu, Weici; Arieno, Marcus; Löw, Henrik; Huang, Kaifang; Xie, Xiulan; Cruchter, Thomas; Ma, Qiao; Xi, Jianwei; Huang, Biao; Wiest, Olaf; Gong, Lei. Metal-Templated Design: Enantioselective Hydrogen-Bond-Driven Catalysis Requiring Only Parts-per-Million Catalyst Loading. Journal of the American Chemical Society. 2016-07-20, 138 (28): 8774–8780. ISSN 0002-7863. PMC 8103658
 . PMID 27336458. doi:10.1021/jacs.6b02769 (英语).
. PMID 27336458. doi:10.1021/jacs.6b02769 (英语).
- ^ Schreiner, Peter R. Metal-free organocatalysis through explicit hydrogen-bonding interactions. Chem. Soc. Rev. 2003, 32 (5): 289–296. PMID 14518182. doi:10.1039/B107298F.
- ^ Jacobsen, E. N. Asymmetric catalysis with chiral H-bond donors (PDF). [2012-12-18].
- ^ Jacobsen, E. N.; Dustin, J. M.; Zuend, S. J. Catalytic asymmetric total synthesis of (+)-Yohimbine. Org. Lett. November 2008, 10 (5): 745–748. PMID 18257582. doi:10.1021/ol702781q.
- ^ Takemoto, Yoshiji; Miyabe, H. Discovery and application of asymmetric reaction by multi-functional thioureas. Bull. Chem. Soc. Jpn. July 2008, 81 (7): 785–795. doi:10.1246/bcsj.81.785
 .
.
- ^ Zuend, S. J.; Coughlin, M. P.; Lalonde, M. P.; Jacobsen, E. N. Scaleable [sic] catalytic asymmetric Strecker syntheses of unnatural alpha-amino acids. Nature. October 2009, 461 (7266): 968–970. Bibcode:2009Natur.461..968Z. PMC 2778849
 . PMID 19829379. doi:10.1038/nature08484.
. PMID 19829379. doi:10.1038/nature08484.
